Всё чаще в современном мире рождение первенца откладывается женщинами до момента достижения определенного уровня жизни и успеха. В России средний возраст рождения первого ребенка составляет 28 лет. В некоторых странах Европы этот возраст соответствует 31 году.
В связи с тенденцией к откладыванию материнства медицина активно изучает способы определения потенциала фертильности женщины – то есть способности конкретной женщины к зачатию.
Оценка овариального резерва входит в обследование пары при бесплодии, невынашивании беременности, планировании беременности и для оценки прогноза фертильности женщины.
Что такое овариальный резерв?
Одним из методов определения фертильности женщины является оценка овариального резерва (резерв или запас яичников). Однако нужно понимать, что не всегда высокий овариальный резерв гарантирует быстрое наступление беременности, и наоборот, женщины с крайне низким овариальным резервом вовсе не лишены способности к зачатию.
Это связано с тем, что овариальный резерв – это генетически заложенный запас фолликулов в яичниках, а для наступления беременности необходимо не только наличие фолликула, но и слаженная работа гормональной системы, яичников, маточных труб и матки, а также важно качество сперматозоидов.
Именно поэтому, оценив только лишь овариальный резерв, нельзя сделать точный прогноз на наступление беременности.
Фолликулогенез
Фолликулогенез – это процесс развития фолликулов (и яйцеклеток) в яичнике.
Формирование женских половых клеток начинается ещё до момента рождения.
Во время эмбрионального периода развития плода образуются первичные половые клетки, которые многократно делятся путем митоза, образуя оогонии, а затем образуются ооциты первого порядка, которые содержат диплоидный набор хромосом (46 хромосом или 23 пары). Ооциты первого порядка, окруженные одним слоем клеток гранулезной оболочки, образуют примордиальные фолликулы.
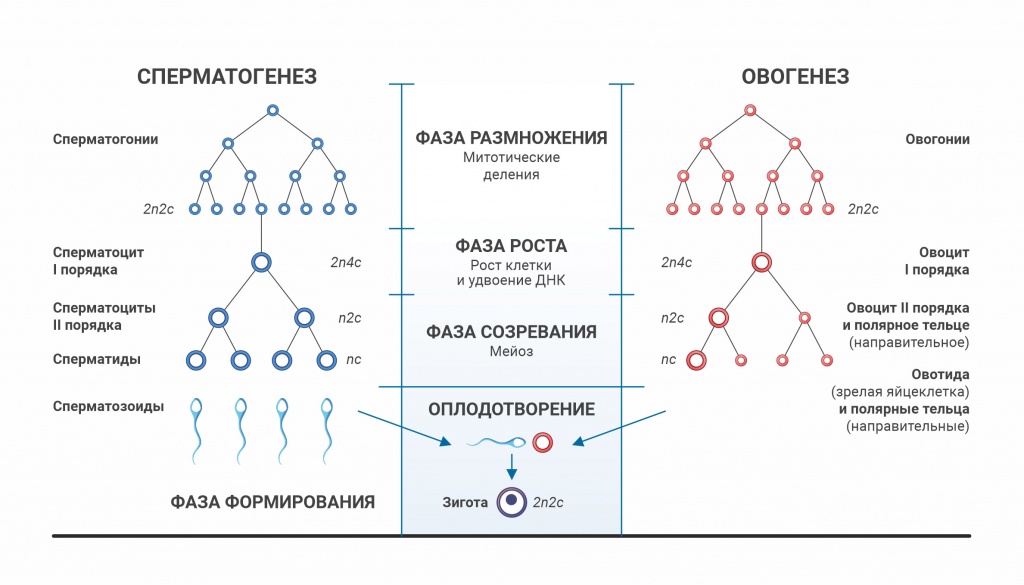
Именно количество примордиальных фолликулов (примордиальный пул) в яичнике определяет овариальный резерв.
Сколько яйцеклеток у женщины?
К моменту начала менструации в яичнике девочки в норме находится около 270 000 – 470 000 фолликулов. И только 300 - 500 из них продолжат своё развитие до стадии ооцитов второго порядка (т.е. достигнут овуляции), а остальная часть подвергнется атрезии на различных этапах развития.
Процесс уменьшения количества яйцеклеток начинается еще во внутриутробном периоде развития девочки и продолжается до менопаузы. Этот процесс невозможно замедлить, атрезия продолжается даже на фоне беременности, лактации и приёма оральных контрацептивов. А также, вопреки всем мифам, этот процесс невозможно ускорить путем стимуляции овуляции и ЭКО. Это связано с тем, что на ранней стадии развития фолликулы не чувствительны к гормонам организма и вводимые гормональные препараты не оказывают на них влияния.
Периоды фолликулогенеза
- Гормон-независимый период. Фолликулы растут от стадии примордиального до стадии вторичного (преантрального) в условиях отсутствия гипофизарных гормонов. Этот период длительный и в настоящее время нет каких-либо маркёров, которые могли бы дать характеристику этой фазы у конкретной женщины.
- Гормон-чувствительная фаза. Фолликулы растут при базальных уровнях гипофизарных гормонов, от стадии вторичного (преантрального) до стадии антрального, размер которого составляет 1-2 мм в диаметре. Этот период длится примерно 100-120 дней (3-4 менструальных цикла). Получить информацию о количестве данного пула фолликулов можно по уровню АМГ в крови – поскольку именно этот гормон выделяется клетками гранулёзы фолликулов в течение всего гормон-чувствительного периода, т.е. уровень этого гормона определяется числом фолликулов на данной стадии роста.
- Гормонозависимый период. Начинается в конце второй фазы менструального цикла – начинает формироваться группа фолликулов, которые под действием гипофизарных гормонов (особенно ФСГ) вырастают от стадии большого антрального в преовуляторные – и достигают момента овуляции. За один цикл только один фолликул достигнет овуляции (редко два или три), остальные подвергаются атрезии. Большинство лабораторных тестов характеризуют именно этот период фолликулогенеза: ФСГ, ЛГ, эстрадиол, ингибин В, а также ультразвуковое определение числа антральных фолликулов и объема яичников.
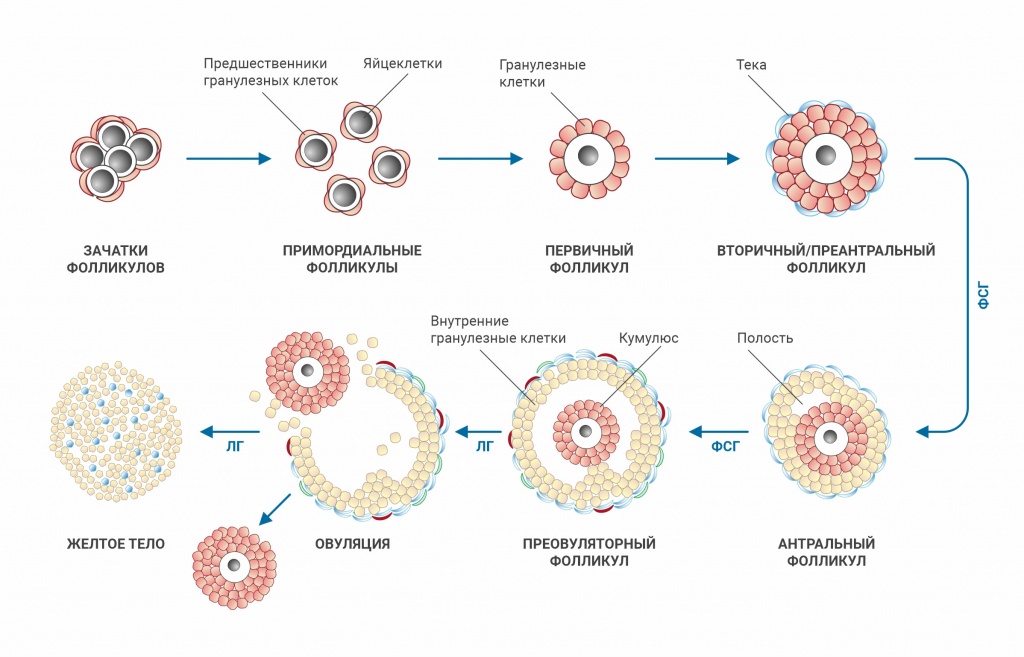
Более подробно о фолликулогенезе и овариальном резерве смотрите в видео И.И.Гузова: Новые способы получения яйцеклеток при истощении овариального резерва.
Маркёры резерва яичников
Возраст
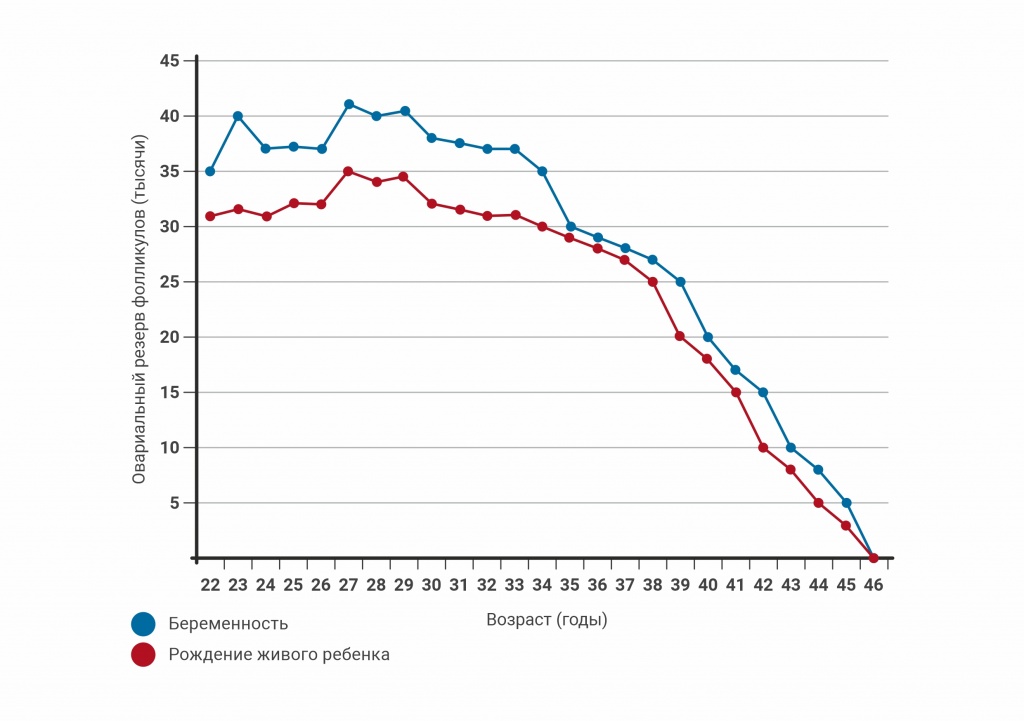
Бесспорно, одним из самых главных факторов, определяющих овариальный резерв, является возраст. Овариальный резерв обратно пропорционален возрасту, то есть, он необратимо снижается с течением времени.
С каждым менструальным циклом общее количество фолликулов уменьшается на всех стадиях роста фолликула и механизмы этих процессов до сих пор хорошо не изучены. Также имеет значение скорость исчезновения фолликулов, которая удваивается при снижении пула примордиальных фолликулов до 25000, что примерно соответствует возрасту 37 лет. Именно после этого возраста овариальный резерв снижается критически.
Важно отметить, что сохранность менструальной функции и даже овуляции не всегда отражает репродуктивный потенциал. Средний возраст менопаузы 51-52 года и до этого периода менструальная функция может быть не нарушена и может случаться овуляция, однако количество естественных беременностей после 42-45 лет крайне низкое.
Старение репродуктивной системы, так же как и воздействие на организм различных факторов среды (ятрогенные, различные интоксикации, курение, алкоголь и т.д), которые вызывают схожие со старением механизмы – могут влиять не только на количество, но и на качество яйцеклеток, поэтому с возрастом также снижается и качество ооцитов.
По одной из теорий качество ооцитов закладывается внутриутробно, и в последующем ооциты, менее подверженные нерасхождению хромосом, овулируют первыми, в то время как ооциты низкого качества достигают овуляции в более позднем периоде жизни женщины. Также имеют значение различные повреждающие воздействия на половые клетки в течение жизни, что приводит к нарушению микроциркуляции, окислительному стрессу, гипоксическим процессам в фолликулярной жидкости.
Антимюллеров гормон - АМГ
Антимюллеров гормон – гормон, который выделяется клетками гранулёзы фолликулов диаметром до 6-8 мм и который отражает количество фолликулов в яичнике на стадии гормон-чувствительного роста.
Этот гормон считается самым ранним и наиболее чувствительным маркером репродуктивного старения, позволяет прогнозировать ответ яичников на гормональную стимуляцию, а также время наступления менопаузы.
Яичники плода женского пола начинают продуцировать АМГ примерно на 36-й неделе беременности. В период полового созревания уровень повышается, достигая пика в возрасте 25 лет, после чего начинает постепенно снижаться практически до нулевых значений в период менопаузы.
Когда сдавать антимюллеров гормон
АМГ можно оценивать в любой день менструального цикла. Уровень гормона совсем незначительно колеблется на протяжении цикла, при этом наибольшие отклонения отмечаются у молодых женщин с более высоким базальным АМГ по сравнению с женщинами старшего репродуктивного возраста, у которых выявляются более низкие базальные уровни АМГ.
Повышение антимюллерова гормона
Уровень гормона напрямую зависит от гинекологических заболеваний и от некоторых внешних факторов. Например, при СПКЯ диагностируются значительно повышенные уровни AMГ, которые коррелируют со степенью выраженности заболевания, а также несут риски гиперстимуляции и многоплодия при проведении стимуляции овуляции.
Причины снижения АМГ
К заболеваниям, снижающим овариальный резерв и уровень АМГ, относится эндометриоз, генетические факторы (например, премутация FMR1), операции на яичниках. У курящих женщин отмечено более раннее снижение уровня АМГ и более раннее начало менопаузы, предположительно, за счет истощения антральных фолликулов. Прием комбинированных оральных контрацептивов может снижать уровень гормона в крови, который возвращается к исходным значениям через 2-4 месяца после отмены препарата.
Что значит и когда сдавать антимюллеров гормон
Исследование уровня АМГ у женщин репродуктивного возраста позволят своевременно диагностировать снижение овариального резерва и ориентировать пациенток на реализацию репродуктивной функции.
Базальный уровень ФСГ и ингибина В
Данные показатели определяются на 2-3 дни менструального цикла.
Под воздействием фолликулостимулирующего гормона гипофиза (ФСГ) фолликулы в яичнике начинают расти, а клетки гранулёзы фолликулов начинают продуцировать ингибин В. Уровень ингибина В коррелирует с количеством фолликулов в яичниках. С возрастом число примордиальных фолликулов резко уменьшается и, следовательно, продукция ингибина снижается, что ведет к повышению ФСГ. Важно отметить, что снижение уровня ингибина В в крови происходит несколько ранее, чем повышение ФСГ, поэтому ингибин В является индикатором начинающегося угасания репродуктивной функции.
Повышение ФСГ более 10-12 МЕ/л говорит о снижении овариального резерва, при этом менструальный цикл может быть не нарушенным. А повышение ФСГ более 25 МЕ/л свидетельствует о приближающейся менопаузе. Такой компенсаторный механизм «заставляет» работать яичники более усиленно, позволяя ещё некоторое время сохранить овуляторную функцию.
Подробнее о гормональном обследовании смотрите видео: Гормоны и оценка овариального резерва
Подсчет антральных фолликулов (AFC)
Antral Follicle Count (AFC) - подсчёт антральных фолликулов – это ультразвуковой метод оценки овариального резерва, во время которого в каждом яичнике считаются фолликулы, имеющие размер от 2 до 10 мм на 2-3-й дни менструального цикла. Также производится измерение объема яичников.
Количество фолликулов более 10-11 в обоих яичниках говорит о сохранном овариальном резерве. Объем яичников в репродуктивном возрасте составляет от 4 до 10см3 и чем меньше фолликулов в яичнике, тем меньше будет его объем.
Более подробно можно прочитать здесь: Подсчёт антральных фолликулов, AFC, овариальный резерв.
EFORT-тест
EFORT-тест — это оценка функционального резерва яичников по их реакции на введение экзогенного фолликулостимулирующего гормона (ФСГ).
Метод основан на двукратном измерении в крови уровней гормонов (ингибина В и АМГ) и оценки их динамики после введения фолликулостимулирующего гормона.
Первый забор крови производится на 3 день цикла. Затем вводится препарат фолликулостимулирующего гормона и через 24 часа производится повторный забор крови на анализы.
В норме после введения гонадотропного препарата уровень АМГ должен снизиться, а концентрация ингибина В — повыситься. При истощении овариального резерва ответ яичников будет недостаточным, поэтому показатели ингибина В и АМГ могут измениться в обратном соотношении или остаться прежними.
Несоответствие показателей овариального резерва
Существует множество показателей для оценки овариального резерва и прогнозирования реакции яичников на стимуляцию. В целом, с возрастом уровни ФСГ повышаются, а уровни АМГ, ингибина В и количества антральных фолликулов (AFC) снижаются. Дополняют картину ингибин B и эстрадиол в раннюю фолликулярную фазу.
В ходе диагностики и лечения у каждой пятой женщины наблюдаются несоответствия в этих показателях. Поэтому для оценки используется не какой-то один маркер, а комплекс исследований, на основании которых делается вывод. Врач учитывает всю картину, включая возраст, акушерский анамнез, заболевания и лечение.
В исследовании Gleicher et al. было показано, что реакция на стимуляцию снижалась в следующем порядке: нормальные уровни АМГ и ФСГ, нормальные уровни АМГ, но снижение уровни ФСГ, снижение уровни АМГ, но нормальные уровни ФСГ и снижение АМГ и ФСГ.
Уровень АМГ и количество антральных фолликулов являются двумя наиболее точными показателями для прогнозирования резерва и реакции яичников. Как АМГ, так и AFC показали значительную корреляцию с возрастом и ответом на стимуляцию. Чем выше значение AFC, тем благоприятнее прогноз, даже при снижении АМГ.
Почему существует несоответствие между уровнем AFC и АМГ? Это может быть связано с различиями в популяции фолликулов, представленной двумя показателями. AFC относится к числу фолликулов диаметром от 2 мм до 9 мм. Они реагируют на гонадотропин и могут развиться в цикле стимуляции.
АМГ же вырабатывается гранулезными клетками преантральных и малых антральных фолликулов диаметром менее 4 мм в яичнике, косвенно отражает популяцию рано растущих фолликулов. Они не способны вступить в стадию набора фолликулов во время цикла индукции овуляции. Следовательно, уровень АМГ в основном отражает резервную функцию яичников.
Факторы, снижающие овариальный резерв
Воспалительные заболевания органов малого таза
Воспалительные заболевания органов малого таза иногда сопровождаются выраженным спаечным процессом, склерозом тканей, в том числе тканей яичников. Происходит нарушение питания яичникового фолликулярного аппарата, которое может повлечь за собой снижение овариального резерва.
Курение
Курение оказывает значительное негативное влияние на овариальный резерв. У курящих женщин отмечаются повышенные уровни гормона ФСГ, сниженный АМГ и снижение антральных фолликулов в яичниках. Снижение овариального резерва в группах курящих женщин встречается в 3 раза чаще, чем у некурящих пациенток. А время наступления менопаузы у курящих женщин в среднем на 2 года раньше.
Оперативные вмешательства на органах малого таза
Значительную роль в уменьшении овариального резерва играют оперативные вмешательства на яичниках.
Это одна из самых распространенных причин снижения овариального резерва. Любая операция на яичнике – резекция по поводу кисты, эндометриоза, апоплексии – ведет к потере части ткани яичника и к снижению овариального резерва.
Лучевая и химиотерапия
Радиационное и химиотерапевтичекое лечение различных опухолевых заболеваний крайне негативно сказывается на репродуктивной функции. Поэтому, разработка тестов определения овариального резерва позволяет прогнозировать дальнейшую репродуктивную и менструальную функцию у молодых пациенток с онкологическими заболеваниями.
Генитальный эндометриоз
Эндометриоз является одной из ведущих причин женского бесплодия. Эндометриоз III–IV стадии ассоциирован с значительным уменьшением овариального резерва. Это связано не только с поражением эндометриозом непосредственно ткани яичника, но и со значительным объемом резекции яичников, необходимым при хирургическом лечении эндометриодных кист.
Преждевременное истощение яичников
В случае выявления снижения овариального резерва у молодых женщин проводится анализ гена FMR1 – "ломкой" Х-хромосомы. У 21% женщин с премутацией в этом гене может развиваться преждевременная недостаточность яичников и присутствует риск наследственного заболевания сыновей.
Многие эксперты говорят, что уточнение статуса гена FMR1 может быть полезно любой женщине, планирующей беременность.
Несколько часто задаваемых вопросов гинекологу об овариальном резерве
Зачем и кому оценивать овариальный резерв?
Приведённые маркёры оцениваются для прогноза вероятности наступления беременности, оценки функции яичников, для прогнозирования ответа яичников на стимуляцию овуляции, а также обязательно должен оцениваться женщинам с репродуктивными проблемами, бесплодием, нарушением цикла и женщинам, которые по какой-то причине хотят отложить материнство на неопределенный срок.
Когда подозревать снижение овариального резерва?
Снижение овариального резерва это растянутый во времени процесс. Очень часто признаки преждевременного истощения яичников могут отсутствовать долгое время, а когда появляется повод обратиться к врачу – резерв оказывается крайне низким.
Обратиться к врачу нужно:
- Если началось изменение характера менструального цикла: например он удлинился, всё чаще происходят задержки менструации, или они вовсе стали отсутствовать в течение более 3х месяцев. Либо наоборот цикл стал укорачиваться.
- Если есть в анамнезе операции на яичниках, наличие эндометриоза, кист яичников, спаечного процесса в малом тазу.
- Если в семье были случаи раннего наступления менопаузы, преждевременного истощения яичников.
- Если есть проблемы с зачатием, ненаступление беременности в течение 6-12 месяцев.
Какими в норме должны быть маркёры овариального резерва?
Общепринятых четких норм нет, следует оценивать все данные в совокупности, особую роль играет возраст пациентки и её анамнез – длительность бесплодия (если оно есть), наличии сопутствующей гинекологической и экстрагенитальной патологии.
В общих чертах можно выделить следующие группы женщин:
- Нормальный овариальный резерв: регулярный менструальный цикл, уровень ФСГ не более 12 МЕ/л, АМГ более 1.2 нг/мл, количество антральных фолликулов в каждом яичнике более 5, объём яичников более 5 см3.
- Сниженный овариальный резерв: нарушение менструального цикла, его укорочение или удлинение, уровень ФСГ более 12 МЕ/л, АМГ более 0,6, но менее 1,2 нг/мл, объем яичников от 3 до 5 см3, количество антральных фолликулов 3-5 в каждом яичнике.
- Крайне низкий овариальный резерв: стойкие нарушения менструального цикла, олигоменорея, аменорея, повышение ФСГ более 25 МЕ/л, АМГ менее 0,6 нг/мл, объем яичников менее 3 см3, число антральных фолликулов менее двух в каждом яичнике.
Возможна ли естественная беременности при низком овариальном резерве или только ЭКО?
Шансы наступления естественной беременности снижаются, но они есть. Случаев наступления беременности при низком овариальном резерве очень много. По одному показателю овариального резерва нельзя делать прогноз на беременность или направлять на ЭКО. Следует провести полноценное обследование, исключить другие возможные факторы ненаступления беременности, скорректировать их и только после этого принимать решение о необходимости ЭКО у конкретной женщины, исходя из ее возраста, длительности бесплодия и ведущей причины отсутствия беременности.
Можно ли повысить овариальный резерв?
Самая сложная проблема в репродукции – это старший репродуктивный возраст и преждевременное истощение яичников - состояние, при котором значительно уменьшается число антральных фолликулов в яичниках, критично низкий АМГ и высокие цифры ФСГ, возникают задержки менструации или они вовсе отсутствуют. Такое заболевание возникает или вследствие проведенных операций на яичниках с иссечением большого количества ткани, либо же из-за генетических особенностей женщины.
Учеными доказано, что в яичниках таких женщин (даже при отсутствии менструации) всё равно есть фолликулы, но преантральные, «спящие» - на которые нельзя воздействовать гормональными препаратами. Профессор Кавамура разработал уникальную методику воздействия на ткань яичника с преантральными фолликулами, после чего они становятся антральными, т.е. чувствительными к гормональной стимуляции.
Активация яичников по методу Кавамура происходит следующим образом: при лапароскопии проводится забор ткани яичника. А затем в лабораторных условиях производят активацию преантральных фолликулов и проводят обратный перенос активированной ткани в яичник. У женщины даже появляются собственные менструации, как правило, на 1-3 цикла. В этот период проводится программа стимуляции овуляции, и пункции для получения ооцитов с помощью программы ЭКО. К сожалению, только у 50% женщин происходит фолликулярная активация в яичниках, позволяющая получить эмбрионы. А до операции неизвестно, сколько «спящих» фолликулов в яичниках женщины сохранилось и как они реагируют на активацию.
Еще одним методом, положительно сказывающимся на овариальном резерве и улучшающим качество доминантного фолликула является применение низких доз дигидроэпиандростерона (ДГЭА) пациентками старшего репродуктивного возраста. Это происходит потому, что в организме с возрастом происходит дефицит ДГЭА, из которого образуются все андрогены и эстрогены. А для поддержки внутриклеточного механизма выработки тестостерона и эстрадиола возможно введение ДГЭА извне. Положительный эффект наступает через 3-4 месяца после начала приема препарата, что примерно соответствует полному циклу роста фолликулов в яичниках.
Читайте также
Яйцеклетка. Новые способы получения яйцеклеток при истощении овариального резерва. Новости науки.
Список литературы
- Fertility preservation for deferred childbearing for nonmedical indications. Authors: Karine Chung, MD, MSCE Meghan B Smith, MD uptodate.com
- Ovarian development and failure (menopause) in normal women. Author: Corrine K Welt, MD, Section Editors: Robert L Barbieri, MD, William F Crowley, Jr, MD, Deputy Editor: Kathryn A Martin, MD uptodate.com
- Определение референтных интервалов антимюллерова гормона, специфичных для российской популяции © И.И.Гузов , Е.Ю.Печёрина, А.В.Ружанская, В.А.Козлов, О.И. Ласкина, Н.Н.Синтюрина, Е.А.Седышкина, Е.Ю.Гвоздик, С.А.Тё, А.В.Зенкина, А.С. Куранников Лабораторная служба 2019, Т. 8, № 2, с. 25–35
- Боярский К. Ю. Клиническое значение тестов определения овариального резерва в лечении бесплодия / Санкт-Петербург, 2000.
- Боярский К. Ю. Фолликулогенез и современная овариальная стимуляция (обзор литературы) /К. Ю. Боярский // Проблемы репродукции. – 2002.
- Калинина Е. А. Резервы повышения эффективности экстракорпорального оплодотворения при лечении бесплодия у женщин с гинекологическими заболеваниями : Научный центр акушерства, гинекологии и перинатологии РАМН. – М.,2005.
- Мишиева Н. Г. Бесплодие у женщин позднего репродуктивного возраста: принципы диагностики и лечения в зависимости от овариального резерва / ФГУ «Научный центр акушерства, гинекологии и перинатологии им. В. И. Кулакова 2008.
- Количественный анализ состава фолликулов яичника при эндометриозе / Курило Л. Ф. [и др.] // Проблемы репродукции. — 2006.
- Назаренко Т. А., Смирнова А. А. Индукция моно- и суперовуляции: оценка овариального резерва, ультразвуковой и гормональный мониторинг // Проблемы репродукции. 2004.
- Evaluation and management of infertility in females of advancing age. Author: Mary E Morris, MD, PhD uptodate.com





Комментарии
-

Елизавета
01.11.2022 10:36
43 года. Пролактин 318. ФСГ 80, эстрадиол 30,91.
-

Клиники и лаборатории ЦИР
 Клиники и лаборатории ЦИР
Клиники и лаборатории ЦИР
09.11.2022 10:45
Эстрадиол нормальный у вас, то есть он низкий, но, скорее всего, овуляции нет, потому что идет очень высокий фолликулостимулирующий гормон.
-

Аноним
04.11.2022 22:37
40 лет. После свадьбы месячные без таблетки не приходят (фемостон). Сказали, детская матка, вторичная аменорея неясного генеза. ФСГ 66,67, ЛГ 29,61, АМГ 0,01. Есть ли шанс иметь детей?
-

Клиники и лаборатории ЦИР
 Клиники и лаборатории ЦИР
Клиники и лаборатории ЦИР
09.11.2022 10:57
Цифры, которые Вы прислали, указывают на четкие признаки снижения овариального резерва, не соответствующие возрасту. Поэтому здесь мы рекомендуем провести более углубленное обследование. На фоне Фемостона у вас пришла менструация.
Комментарии 1 - 2 из 12В таких случаях мы рекомендуем провести более углублённое гормональное обследование в раннюю фолликулярную фазу. То есть на 3-й и на 8-й день цикла, для того, чтобы у нас было четкое определение фона по целому набору показателей.
И дальше мы назначаем ДГЭА в обычной дозе - 25 мг 2 раза в сутки и смотрим, что происходит. В некоторых случаях возможно улучшение, и даже восстановление, овуляции, всё зависит от того, насколько сохранны ваши яичники.
Через 2-3 месяца смотрим контрольные гормональные показатели в раннюю фолликулярную фазу и в среднюю фолликулярную фазу. И если идет положительная динамика, тогда мы продолжаем эту терапию и рассчитываем на то, что можно что-то восстановить.
Если на ДГЭА реакции не будет, то при таких цифрах ФСГ самостоятельное наступление беременности очень маловероятно.
https://www.youtube.com/watch?v=g7ZIRnFqPdA
Фемостон не принимаете - смотрим набор показателей на 3-й и на 8-й день цикла, просто для того чтобы можно было с чем-то сравнивать. Назначаем ДГЭА по 25 мг 2 раза в сутки, наблюдаем.
Это не для 40 лет показатели, которые вы нам прислали. Поэтому здесь важно посмотреть какие-то дополнительные факторы, которые могут быть причиной того, почему у Вас всё так идёт.
Что посмотреть дополнительно? Это мутации гена FMR1, антиовариальные антитела, нет ли аутоиммунной атаки на яичник.
Посмотреть показатели обмена железа: железо, трансферрин, ферритин и НЖСС. Потому что иногда бывает так, что избыточное железо, которое накапливается в организме, даёт удар по яичнику, гибнут фолликулы. И это состояние, которое характеризуется избытком железа, может начать ломать ваш организм и по другим направлениям.
Эти 3 показателя (мутации гена FMR1, антиовариальные антитела, показатели обмена железа) как дополнительный фактор, который, возможно, позволит понять те причины, из-за которых у Вас так всё это идет.
И на всякий случай в таких ситуациях мы всегда рекомендуем сдать анализ на кариотип (определение хромосомного набора).
https://www.youtube.com/watch?v=OVcNSjQLCN4
Начало | Пред. | 1 2 3 4 5 | След. | Конец