Фактор VII является одним из ключевых факторов в каскаде свертывания крови. Он относится к факторам свертывания крови, зависимым от витамина K. Уяснение роли VII фактора в свертывании крови и значения витамина K для нормальной коагуляции открывает путь к пониманию важнейших механизмов, лежащих в основе поддержания нормальной активности системы гемостаза, и механизмов развития патологии, приводящей к повышению риска кровотечений и тромбозов. Наследственные дефекты генов фактора VII и ферментов, участвующих в превращении витамина K могут влиять не только на риск тромбозов и кровотечений, но и на формирование плаценты и плацентарного кровообращения, риск осложнений беременности. Опыт показывает, что не только пациенты, но и многие врачи испытывают трудности с интерпретацией анализов на полиморфизм генов системы гемостаза. Надеемся, что данная статья окажется полезной врачам и пациентам, поможет улучшить качество подготовки к беременности и ведения беременности у женщин высокого риска осложнений беременности. Еще одной целевой аудиторией данной статьи являются врачи, ведущие пациентов с риском сосудистых и тромботических осложнений (терапевты, кардиологи, хирурги, педиатры).
Свертывание крови в норме является тонко регулируемой системой, обеспечивающей, с одной стороны, поддержание в жидком состонии крови внутри сосудов, но, с другой стороны, быстро включающейся в ответ на повреждение сосудов, предотвращая кровопотерю. Нормальное состояние крови поддерживается разнонаправленными механизмами, одни из которых обеспечивают активацию, а другие - торможение свертывания крови. При избыточной активности механизмов, способствующих коагуляции и при недостаточной активности механизмов, препятсвующих коагуляции появляется риск тромбозов - образование сгустков крови внутри сосудов, затрудняющих нормальное кровообращение. При противоположных ситуациях повышается риск кровотечений.
Фактор VII стоит в самом начале цепочки реакций самоусиления (каскадных реакций), в конечном итоге приводящих к образованию сгустка фибрина. Он был впервые открыт независимо друг от друга двумя группами исследователей в 1949 и в 1951 г. и имеет несколько синонимов, самым распространенным из которых является проконвертин. Фактор VII является гликопротеином, относящимся к группе витамин-K-зависимых сериновых протеаз. Он играет ключевую роль в свертывании крови. Другими витамин K-зависимыми факторами являются протромбин, факторы IX и X, а также протеины C и S.
Активация фактора VII происходит под воздействием тканевого фактора. Тканевой фактор является гликопротеином мембраны клетки, который в нормальных условиях "спрятан" под мембраной и поэтому не экспрессируется на поверхности выстилки сосудов. При повреждении стенки сосуда тканевой фактор попадает в кровь и начинает взаимодействовать с небольшими количествами активного (VIIa) и неактивного (VII) фактора VII. Это соединение резко ускоряет превращение фактора VII в фактор VIIa. Фактор VIIa в соединении с тканевым фактором в присутствии кальция и фосфолипидов облегчает превращение фактора IX в фактор IXa и фактора X в фактор Xa. Такая активация свертывания крови традиционно называется внешним путем активации гемостаза. Таким образом, комплекс фактора VIIa с тканевым фактором является мощным активаторов факторов IX и X.
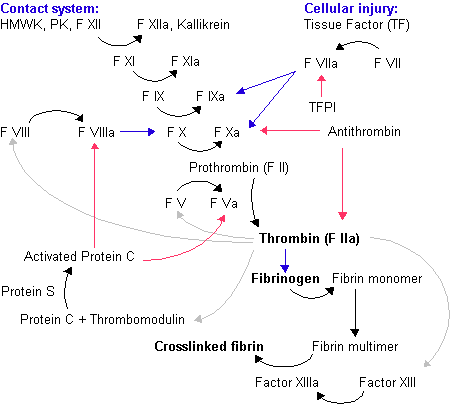
Фактор VII имеет самый короткий период полужизни (6-8 часов) по сравнению со всеми другими факторами свертывания крови, поэтому при возникновении таких проблем, как нарушение функции печени или дефицит витамина K, уровень фактора VII в крови снижается быстрее всех витамин K-зависимых факторов.
Концентрация фактора VII повышается во время беременности у здоровых женщин. Концентрация активного фактора VII у носителей разных генетических вариантов фактора может различаться в несколько раз.
Ген VII фактора расположен на длинном плече 13-й хромосомы (13q34), недалеко от гена фактора X. Фактор VII синтезируется в печени и секретируется в виде гликопротеина, состоящего из одной пептидной цепочки молекулярной массой 48 кД. Подобно остальным витамин K-зависимые зимогенам фактор VII имеет Gla-домен, каталитический домен и домены, подобные эпидермальному фактору роста.
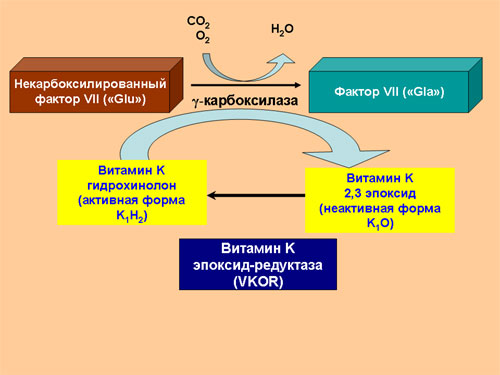
Аббревиатура Gla обозначает остаток гамма-карбоксиглутаминовой кислоты (gamma-carboxyglutamic acid). В синтезируемой внутри клетки белковой цепи фактора VII на N-конце находится 34 остатка глутаминовой кислоты (Glu). После завершения синтеза белка внутри клетки происходит карбоксилирование 10 таких остатков, в результате чего остатки глутаминовой кислоты превращаются в остатки гамма-карбоксиглутаминовой кислоты. Такая модификация белка называется посттрансляционным модифицированием. Пострансляционное модифицирование фактора VII происходит под действием фермента гамма-карбоксилазы в присутствии активной формы витамина K. В результате этой реакции витамин K выступает донором атомов водорода и превращается в неактивную окисленную форму (эпоксид витамина K). Обратное превращение неактивной формы витамина K в активную происходит под действием фермента витамин-K-эпоксид-редуктазы (VKOR, vitamin K oxoreductase). При дефиците витамина K и при снижении активности VKOR нарушается карбоксилирование всех витамин K-зависимых факторов свертывающей и противосвертывающей системы, что резко нарушает их функционирование, поскольку Gla-домен отвечает за взаимодействие факторов свертывания крови с фосфолипидами мембран.
Каталитический домен отвечает за ферментную активность фактора VII, а 2 домена, сходных с эпидермальным фактором роста отвечают за связь фактора VII с ионами кальция. В таком виде неактивный фактор VII поступает в кровь из печени. Активация фактора VII (превращение профермента (=зимогена) в активный фермент, обозначаемый аббревиатурой VIIa происходит в результате разрезания пептидной связи между остатком аргинина (Arg, R) в позиции 323 и остатком изолейцина (Ile, I) в позиции 324.
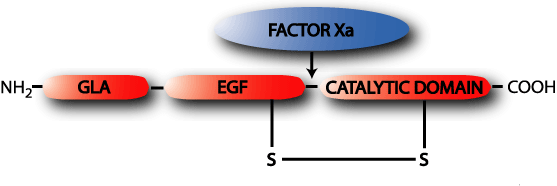
Итак, разрезание пептидной связи между остатком аргинина 152 и остатком изолейцина 153 приводит к образованию активной формы фактора VII (VIIa). В результате из N-конца пептидной цепочки образуется легкая цепь (мол. масса около 20000, а из C-конца - тяжелая цепь (мол. масса около 30000). Обе цепи остаются ковалентно связанными дисульфидным мосткиком. из N-
Быстрая активация происходит после соединения неактивного фактора VII со своим кофактором (тканевым фактором) в присутствии ионов кальция.
К настоящему времени описано несколько полиморфизмов фактора VII. Большинство полиморфных вариантов приводят к снижению секреции фактора VII в кровь и к снижению активности фактора VII. Уровень антигена фактора VII в крови, отражающий общую концентрацию фактора обычно обозначается аббревиатурой VII:Ag (от слова antigen), а коагулянтная активность фактора, которая может не совпадать с концентрацией антигена - аббревиатурой VII:C (от слова coagulation, свертывание).
Полиморфизм Arg353Gln заключается в замене аргинина на глутамин в позиции 353. В системе однобуквенных кодов аминокислот, предложенной в начале 1960-х годов биохимиком Джоржтаунского университета Маргарет Оукли Дейхофф аргинин обозначается буквой R, а глутамин - буквой Q. Поэтому в литературе этот полиморфизм обозначается также как R353Q. Это одно и то же. Замена одной аминокислоты на другую в цепочке белка обусловлено точечной заменой в позиции 10976 цепочки гена одного азотистого основания (гуанина, G) на другое азотистое основание (аденин, A). Поэтому тот же самый полиморфизм может обозначаться как G10976A. Наличие варианта Gln в гетерозиготном состоянии (R/Q) приводит к снижению концентрации и активности фактора VII в крови на примерно на 25%, а наличие гомозиготности Q/Q - к снижению концентрации и активности фактора примерно на 50% по сравнению с обычными носителями варианта R/R. Данный полиморфизм был впервые описан Green и сотр. в 1991 г.
Концентрация фактора VII в крови находится под влиянием большого количества генетических факторов и факторов внешней среды. Последние включают в себя количество жиров в диете, возраст, наличие ожирения, наличие сахарного диабета, у женщин - начало менопаузы и назначение гормональной заместительной терапии. Концентрация фактора VII в крови хорошо коррелирует с уровнем триглицеридов. Чем выше уровень триглицеридов в крови, тем выше концентрация фактора VII.
Повышение концентрации фактора VII в крови сопровождается повышением риска таких заболеваний, как инфаркт миокарда и гипертоническая болезнь. В случае инфаркта миокарда вероятность летального исхода значительно повышается при высоких концентрациях фактора VII в крови. Во время беременности риск осложнений, связанных с нарушением функции плаценты бывает тем выше, чем выше концентрация фактора VII. Высокие концентрации фактора VII сопровождаются значительным повышением риска тромботических осложнений у женщин на фоне гормональной контрацепции и гормональной заместительной терапии, особенно в сочетании с курением, ожирением и сахарным диабетом.
Исследования последних лет показали, что наличие вариантов Q/Q и R/Q значительно снижает риск возникновения и тяжелого исхода инфаркта миокарда и гипертонической болезни. Более частый вариант R/R, наоборот, является дополнительным фактором риска сосудистых осложнений.
Многие осложнения беременности, сопровождающиеся риском нарушения плацентарной функции (остановка развития беременности на малых сроках, задержка внутриутробного развития, гипотрофия плода, фето-плацентарная недостаточность, некоторые виды аномалий внутриутробного развития плода) связаны с повышением риска тромбозов спиральных артерий. Ситуация усугубляется физиологическим повышением факторов свертывания крови при беременности, таких как фактор II (фибриноген) и фактор VII. Это объясняет интерес акушеров-гинекологов к полиморфизму фактора VII у беременных женщин и к включению определения данного полиморфизма при обследовании при осложненном течении беременности и после многократных неудачных попыток ЭКО. Л. А. Никитина и сотр. (2007) показали, что наличие варианта Gln снижает риск неблагоприятного исхода беременности. Было также установлено, что наличие генотипа R/R у внутриутробного плода является фактором риска атрезии тонкой кишки. Это связано с повышением риска тромбирования сосудов брыжейки у плода, что является одной из важных причин атрезии тонкой кишки (Johnson и Meyers, 2001). Сочетание варианта R/R c лейденской мутацией еще больше повышают риск атрезии тонкого кишки. Для выяснения риска повторения подобных осложнений беременности может потребоваться обследование мужа на полиморфизм генов гемостаза с целью прогнозирования вариантов генотипа плода.
 Витамин K был открыт датским исследователем Хенриком Дамом в процессе исследований 1929 - 1935 гг., получившим в 1943 году вместе с американским исследователем Эдвардом Дойзи Нобелевскую премию за открытие и исследование свойств витамина K. Дам изучал метаболизм холестерина и для выяснения влияния питания на синтез холестерина в организме проводил опыты на цыплятах, которым давали специальную обезжиренную диету. Цыплята заболевали неизвестной болезнью, если такая диета продолжалась более 2-3 недель. У них возникали множественные кровоизлияния под кожей, в мышцах и внутренних органах, а кровь свертывалась очень медленно. Болезнь возникала в результате нехватки неизвестного химического вещества, которое не совпадало ни с одним из известных к тому времени витаминов. Как сам Дам рассказал в своей Нобелевской лекции, он был назван витамином K по немецко-скандинавскому слову Koagulation (свертывание) и оказался первым витамином, названным от неанглийского слова.
Витамин K был открыт датским исследователем Хенриком Дамом в процессе исследований 1929 - 1935 гг., получившим в 1943 году вместе с американским исследователем Эдвардом Дойзи Нобелевскую премию за открытие и исследование свойств витамина K. Дам изучал метаболизм холестерина и для выяснения влияния питания на синтез холестерина в организме проводил опыты на цыплятах, которым давали специальную обезжиренную диету. Цыплята заболевали неизвестной болезнью, если такая диета продолжалась более 2-3 недель. У них возникали множественные кровоизлияния под кожей, в мышцах и внутренних органах, а кровь свертывалась очень медленно. Болезнь возникала в результате нехватки неизвестного химического вещества, которое не совпадало ни с одним из известных к тому времени витаминов. Как сам Дам рассказал в своей Нобелевской лекции, он был назван витамином K по немецко-скандинавскому слову Koagulation (свертывание) и оказался первым витамином, названным от неанглийского слова.
Витамин K включает в себя группу жирорастворимых витаминов, которые необходимы для посттрансляционной модификации нескольких белков, большинство которых является белками свертывающей и противосвертывающей системы крови. Химически они относятся к производным 2-метил-1, 4 нафтохинолона.
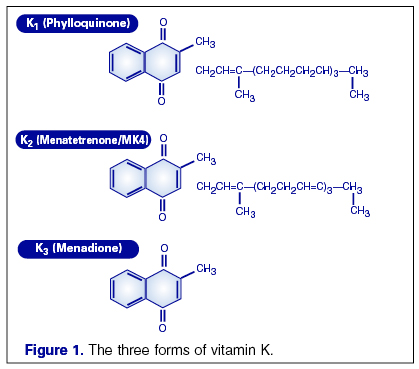
Все члены семейства витамина K имеют метилированное нафтохинолоновое кольцо и боковую цепь, содержащую различное число остатков изопрена. Филлохинолон (витамин K1) имеет 4 остатка изопрена в боковой цепи, один из которых ненасыщен. Менахинолоны (витамин K2) содержат различное количество ненасыщенных остатков изопрена. Обычно они обозначаются как MK-n, где n - число остатков изпорена. Наличие остатков изопрена сближает витамины K с другими жирорастворимыми витаминами (A, E и убихинолоны (коэнзимы Q)). Витамины K1 и K2 являются единственными природными витаминами K. Остальные витамины K (K3, K4 и т. д.) являются синтетическими препаратами.
Витамин K1 содержится в зеленых овощах (шпинат, латук, цветная капуста, злаках, авокадо, киви, бананах, в мясе, молочных продуктах, яцах, сое, растительных маслах, в частности, в оливковом масле. Витамин K2 сннтезируется бактериями кишечника, поэтому авитаминоз витамина K у взрослых - редкое являение, в основном - при дисбактериозах после лечения антибиотиками. Однако у маленьких детей, у которых кишечник еще не заселен бактериями в достаточном количестве, нередко наблюдается гиповитаминоз K, который может давать склонность к кровотечениям. Витамин K не проникает через плаценту.
Как указывалось выше, витамин K необходим для карбоксилирования остатков глутаминовой кислоты в некоторых белках, которые превращаются в остатки гамма-карбоксиглутаминовой кислоты (Gla). Белки, которые претерпевают такую посттрансляционную модификацию называются Gla-белками.
У человека известно 14 Gla-белков:
Ген VKORC1 кодирует субъединицу 1 комплекса эпоксид-редуктазы витамина K. Это мембранный протеин, состоящий из одной пептидной цепи, состоящей из 163 аминокислотных остатков, тесно связанный с эндоплазматическим ретикулумом. Как было показано выше, этот фермент переводит неактивную (окисленную) форму витамина K, поступающую в организм, в активную (редуцированную) форму, участвующие в пострансляционном карбоксилировании витамин K-зависимых белков. Дефицит фермента может приводить к тотальному снижению активности всех витамин-K-зависимых факторов.
Как и ожидалось, наибольшая концентрация VKORC1 была обнаружена в клетках печени, в которой синтезируются факторы свертывания крови. Однако активность фермента не ограничивается только клетками печени. Значительная активность была обнаружена и в клетках сосудистой стенки, костной ткани, в плаценте, пуповине и других тканях плода.
Огромный интерес к гену VKORC1 возник после того, как выяснилось, что полиморфизм гена, проявляющийся в виде замены остатка цитозина (C) на остаток тимина (T) в позиции 1173 (первый интрон гена) объясняет различия действия непрямых антикоагулянтов на организм. Было давно замечено, что существует 3 группы людей, с существенными различиями в эффективной дозе непрямых антикоагулянтов. В группу A входят пациенты, требующие минимальной дозы препаратов для достижения клинического эффекта, в группу B - пациенты, которым требуется значительно большая доза и группа AB, которым требуется промежуточная доза. Долгое время было непонятно, с чем связаны такие различия. Возможным объяснением было то, что у разных людей разрушение непрямых антикоагулянтов в организме происходит с разной скоростью. И действительно, был обнаружен полиморфизм в гене фермента, участвующего в разрушении непрямых антикоагулянтов (CYP2C9), частично объясняющим такие различия, однако полностью явление разной чувствительности к непрямым антикоагулянтам оставалось неясным. И только открытие полиморфизма VKORC1 C1173T все расставило по местам. Оказалось, что у людей, являющихся носителями генотипа T/T скорость синтеза, а потому и концентрация фермента внутри клетки минимальная. Поэтому для блокады работы фермента требуются малые дозы препаратов. У людей, имеющих генотип C/C скорость транскрипции гена максимальная, а потому и для блокады фермента требуются большие дозировки. Людям с генотипом C/T требуются промежуточные дозы непрямых антикоагулянтов.
Это открытие поистине произвело революцию в назначении этих препаратов, являющимися одними из важных в лечении и профилактике тромбозов, инфарктов и других сосудистых осложнений. У врачей появился метод прогнозирования оптимальной дозы препарата еще до его назначения. Это позволяет значительно улучшить прогноз лечения: выбрать дозу, адекватно понижающую избыточную свертываемость крови и не создать риска кровотечения. Американское агентство FDA включило исследование полиморфизма VKORC1 в число рекомендуемых перед назначением лечения непрямыми антикоагулянтами.
Дальнейшие исследования позволили предположить роль полиморфизма VKORC1 не только в чувствительности организма к непрямым антикоагулянтам, но и плане возможной предрасположенности к развитию других заболеваний, в частности к венозным тромбозам. По предварительным данным (Circulation 2006; 113: 1615-1621) наличие гаплотипа СС может удваивать риск инфаркта миокарда или инсульта. По данным недавнего французского исследования (Lacut и сотр., октябрь 2007)
Может оказаться, что значение полиморфизма VKORC1 выходит за рамки только подбора дозы оральных антикоагулянтов, поскольку фермент участвует не только в регуляции гемостаза, но и в апоптозе (программируемой смерти клетки), развитии костей, кальцинировании стенки артерий, проведении сигнала и контроле роста. Внимание акушеров должен обратить тот факт, что по предварительным данным вариант C/C в значительно большей степени предрасполагает к образованию кальцинатов в стенке артерий (Teichert M. и сотр., январь 2008). Скорее всего, в ближайшее время будут проведены исследования о возможной связи старения плаценты и образования в ней кальцинатов с полиморфизмом гена VKORС1.
Отдельная тема, почти не исследованная на сегодняшний день - это значение полиморфизма VKORC1 для риска осложнений беременности. Было показано, что высокая активность фермента внутри клеток коррелирует с пролиферацией, миграцией, адгезией и формированием сосудистой сети клеток эндотелия пуповины (Wang и сотр., 2006). Можно предположить, что наличие вариантных генотипов VKORC1 у плода может влиять на плацентацию и ангиогенез в плаценте. Вариант C/C является неблагоприятным вариантом в случае дефицита витамина K в организме. Дефицит витамина K у беременных обнаруживается довольно редко, однако не исключен. Вероятность его повышается в случае неправильной диеты, после лечения антибиотиками, при хронических заболеваниях печени. В марте 2005 г. французские авторы (Jessica Jaillet и сотр.) опубликовали случай рождения ребенка с синдромом Биндера (неправильное формирование носа и верхней челюсти) у женщины с желчекаменной болезнью и доказанным дефицитом витамина K в первом триместре. В 11 недель беременности у женщины было обнаружено снижение факторов II, VII, X свертывания крови, а также удлинение протромбинового времени, характерных признаков дефицита витамина K. Хотя это единственный опубликованный на сегодняшний день случай, он не должен пройти без внимания врачей акушеров-гинекологов. При наличии дисбактериоза или других факторов риска дефицита витамина K женщинам с генотипом C/C можно было предложить несколько инъекций витамина K на этапе подготовки к беременности.
Мы затронули одну из важных тем современной медицины: значение генов витамин-K-зависимых факторов для здоровья и болезни. Возможности современной лабораторной диагностики позволяют выяснить конфигурацию генов у человека и на основе этой конфигурации разработать меры по профилактике заболеваний и продлению жизни человека, обеспечению здоровья потомства. Данная статья является продолжением наших публикаций по геномике и молекулярной генетике: